
2026年4月16日,中国药科大学附属南京天印山医院成功召开了“评估BB102片在FGF19过表达的晚期肝细胞癌(HCC)患者中的疗效和安全性的多中心II期临床研究”项目启动会。本次会议由国际国内著名临床肿瘤专家秦叔逵教授与机构办公室主任陈映霞教授共同主持,申办方北京伯汇生物技术有限公司董事长张兴民及研发团队、CRO北京卓越未来国际医药科技发展有限公司代表、机构管理人员以及主要研究者寻琛主任团队共同参与,就试验方案的具体细节与执行流程进行了深入研讨和系统培训。

本项临床试验由复旦大学附属中山医院和安徽省立医院共同担任组长单位,周俭教授与刘连新教授担任Co-Leading PI。秦叔逵教授在开场致辞中剖析了当前晚期肝癌的治疗格局:尽管以免疫治疗为基础的联合方案已成为一线标准,但后线治疗选择依然有限,存在显著的未满足临床需求。FGF19/FGFR4信号通路是驱动肝癌发生发展的重要机制之一,其靶向药物的开发具有重要临床意义。本试验将严格筛选FGF19高表达晚期肝癌患者,科学评估BB102片单药或联合治疗的疗效与安全性,探索基于生物标志物和疗效之间的关系。同时申办方北京伯汇生物技术有限公司张兴民董事长特别致谢南京天印山医院研究团队对本次创新药物临床研究的大力支持与高效推动,期待通过医企双方的紧密合作,共同加速BB102片的临床转化进程,早日造福肝癌患者。

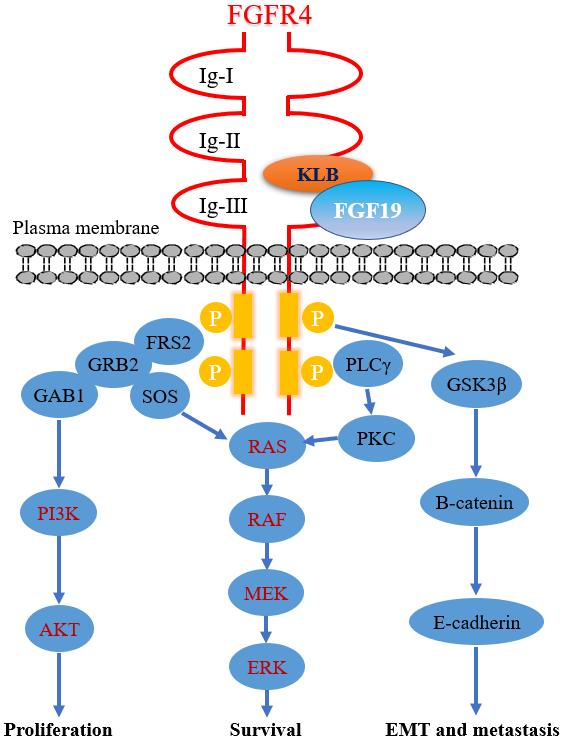
BB102片属于化学药品1类新药,是一种口服的新一代、高选择性、共价可逆的FGFR4抑制剂。其作用机制是通过特异性且强力地抑制肿瘤细胞中的FGFR4蛋白功能,进而阻断FGF19配体与FGFR4受体结合后所驱动的下游促增殖信号通路,从而抑制肿瘤生长。临床前及I期临床研究数据显示,BB102片在FGF19过表达的肝癌模型中表现出显著的抗肿瘤活性,并在早期临床试验中展现了可控的安全性特征,为本次II期临床研究的开展奠定了坚实基础。
在会议研讨环节,各方围绕试验方案的核心与执行细节进行了充分沟通:
01.试验方案设计:明确了本研究为开放标签、多中心II期研究,主要目标人群为经中心实验室检测确认为FGF19过表达、且二线及以上系统性治疗失败的晚期HCC患者。主要终点指标为独立阅片中心(IRC)根据RECISTv1.1进行评估的客观缓解率(ORR)。
02.关键执行要点:研究人员与申办方、CRO团队就具体的入排标准、FGF19检测流程、试验用药剂量(基于I期数据确定的推荐剂量)、治疗期间剂量调整原则、安全性监测以及生物样本采集转运规范等操作细节进行了逐一梳理和确认。
03.质量与合规要求:会议再次强调了遵循GCP原则、严格履行知情同意、确保原始数据记录准确及时的重要性,以保障受试者权益与研究数据的真实可靠。

会议最后,机构办公室陈映霞主任作总结致辞。她指出,BB102片作为一款具有新颖作用机制的国产创新靶向药物,其临床研究具有重要意义。南京天印山医院临床试验机构具备完善的试验管理体系和丰富的项目经验,本次作为参研中心之一,研究团队将恪守研究规范,与申办方及各兄弟中心精诚协作,积极推进并高质量完成本项目,旨在为FGF19阳性的晚期肝癌患者探寻新的有效治疗手段。
素材来源:付康 张如梦
编辑:吴文祺
审核:陈映霞 李勇